
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Senast ändrad 2025-01-22 17:10.
Kollisionsteori , teori används för att förutsäga priserna på kemiska reaktioner , särskilt för gaser. De kollisionsteori bygger på antagandet att för en reaktion för att inträffa är det nödvändigt att de reagerande arterna (atomer eller molekyler) kommer samman eller kollidera med varandra.
Dessutom, vilka är de tre delarna av kollisionsteorin?
Det finns tre Viktig delar till kollisionsteori , att reagerande ämnen måste kollidera , att de måste kollidera med tillräckligt med energi och att de måste kollidera med rätt orientering.
Man kan också fråga sig, hur gör man kollisionsteori? När en katalysator är inblandad i kollision mellan reaktantmolekylerna krävs mindre energi för att den kemiska förändringen ska ta plats, och därmed mer kollisioner har tillräcklig energi för att reaktionen ska inträffa. Reaktionshastigheten ökar därför. Kollisionsteori är nära relaterat till kemisk kinetik.
hur förklarar kollisionsteorin hastigheten för den kemiska reaktionen?
De kollisionsteori säger att kemisk reaktion bara uppstå om det finns kollisioner av rätt energinivåer mellan molekyler och atomer. Det följer att om molekylerna kollidera oftare att detta kommer att öka Betygsätta av reaktion . Ju högre temperatur desto mer kinetisk energi har molekyler och atomer.
Vad är en lyckad kollision inom kemi?
Molekyler måste kollidera med tillräcklig energi, känd som aktiveringsenergin, så att kemisk bindningar kan gå sönder. Molekyler måste kollidera med rätt orientering. A kollision som uppfyller dessa två kriterier, och som resulterar i en kemisk reaktion, är känd som en lyckad kollision eller en effektiv kollision.
Rekommenderad:
Vad skulle hända om det inte fanns några kemiska reaktioner?

Utan kemiska reaktioner skulle ingenting någonsin förändras. Atomer skulle förbli atomer. Nya molekyler skulle inte bildas. Inga organismer kunde leva
Vilket av följande måste uppfyllas för att kollisionsteorin om reaktionshastigheter ska hålla?

Vilket av följande måste uppfyllas för att kollisionsteorin om reaktionshastigheter ska hålla? - De reagerande molekylerna måste kollidera med varandra. – Molekylerna måste kollidera i en orientering som kan leda till omlagring av atomerna. -De reagerande molekylerna måste kollidera med tillräcklig energi
Vad är sant om kemiska reaktioner?

I en kemisk reaktion kan endast de atomer som finns i reaktanterna hamna i produkterna. Inga nya atomer skapas, och inga atomer förstörs. I en kemisk reaktion kommer reaktanter i kontakt med varandra, bindningar mellan atomer i reaktanterna bryts och atomer omarrangeras och bildar nya bindningar för att göra produkterna
Vad är kemiska symboler och kemiska formler?
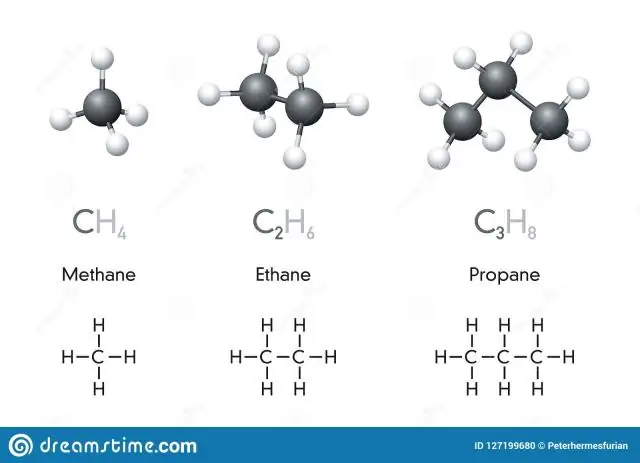
En kemisk symbol är en beteckning på en eller två bokstäver för ett element. Föreningar är kombinationer av två eller fler element. En kemisk formel är ett uttryck som visar grundämnena i en förening och de relativa proportionerna av dessa grundämnen. Många element har symboler som kommer från det latinska namnet för elementet
Vad kan användas för att bestämma hastigheten för enzymkatalyserade reaktioner?

Enzymkatalys detekteras genom att antingen mäta produktens utseende eller försvinnandet av reaktanter. För att mäta något måste du kunna se det. Enzymanalyser är tester utvecklade för att mäta enzymaktivitet genom att mäta förändringen i koncentrationen av en detekterbar substans
