
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Senast ändrad 2025-06-01 05:06.
Varje orbital innehåller två elektroner. π4 ochπ5 är degenererade antibindande orbitaler med två knutpunkter i rät vinkel mot varandra. π6 är en antibindande orbital med tre knutpunkter.
Hur många noder har då en sigma-antibindande orbital?
De anti-bonding sigma sid orbitaler har tre nodplan. De sigma p bindning orbital är den lägsta energin orbital vilket betyder att den kommer att ha noll knutpunkter . Sedan finns det pi-bindningen orbitaler (1 nod ), pi anti-bindande orbitaler (2 knutpunkter ) och slutligen anti-bonding sigma sid orbital som har tre knutpunkter.
hur många noder finns i den molekylära orbitalen med högst energi? De högsta energi nivå ("takvåningen" i vår byggnad) har (n-1) knutpunkter . Vi såg att för butadien (n=4) den högsta energi nivå har tre knutpunkter mellan orbitaler (märkt här med röda streck).
På samma sätt, vad är noder i molekylära orbitaler?
Orbital nod ( nod ): En punkt eller ett plan med noll elektrondensitet i en orbital . Alltid kantad av två eller fler orbital lober. π orbital av eten har två orbital lober (en visas i rött och den andra i blått), och en orbital nod (planet som innehåller teatomer).
Hur många nodplan finns i 2p orbital?
Varje 2p orbital har två lober. Det finns en planarnod vinkelrät mot axeln orbital (alltså 2p x orbital har ett yz nodalplan , till exempel).
Rekommenderad:
Hur många EcoRI-ställen finns det i lambda-DNA?
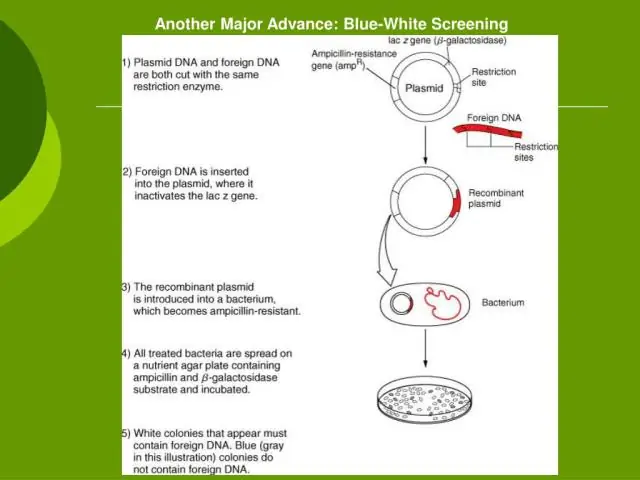
Lambda-DNA som används i detta experiment isoleras som en linjär molekyl från E. coli-bakteriofagen lambda. Den innehåller cirka 49 000 baspar och har 5 igenkänningsställen för Eco RI och 7 för Hind III
Hur vet man hur många elektroner som finns i koppar?

Namn Koppar atommassa 63.546 atommassa enheter Antal protoner 29 Antal neutroner 35 Antal elektroner 29
Hur många radiella noder finns det i en 4s orbital?

Antalet noder är relaterat till det huvudsakliga kvanttalet, n. ns-orbitalen har (n-1) radiella noder, så 4s-orbitalen har (4-1) = 3 noder, som visas i diagrammet ovan
Hur vet man hur många orbitaler som finns i ett skal?

Antalet orbitaler i ett skal är kvadraten på det huvudsakliga kvanttalet: 12 = 1,22 = 4, 32 = 9. Det finns en orbitaler i ett underskal (l = 0), tre orbitaler i ett underskal (l= 1) , och fem orbitaler i ad subshell (l = 2). Antalet orbitaler i ett underskal är därför 2(l) +1
Hur många genkombinationer är möjliga i könsceller produktion för en dihybrid korsning Varför så många?

Möjliga könsceller för varje AaBb-förälder Eftersom varje förälder har fyra olika kombinationer av alleler i könscellerna, finns det sexton möjliga kombinationer för denna korsning
