
Innehållsförteckning:
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Senast ändrad 2025-01-22 17:10.
Använd formeln ∆H = m x s x ∆T för att lösa.
När du har m, massan av dina reaktanter, s, den specifika värme av din produkt och ∆T, temperaturen förändra från din reaktion är du beredd att hitta entalpi reaktion. Anslut bara dina värden till formeln ∆H = m x s x ∆T och multiplicera för att lösa.
Med hänsyn till detta, hur beräknar man energiförändring i kemi?
För att beräkna en energiförändring för en reaktion:
- addera bindningsenergierna för alla bindningar i reaktanterna - detta är "energin i"
- lägga samman bindningsenergierna för alla bindningar i produkterna - detta är "energin ut"
- energiförändring = energi in - energi ut.
Man kan också fråga sig, vad är Q MC _firxam_#8710; T används för? F = mc∆T . F = värmeenergi (Joule, J) m = massa av ett ämne (kg) c = specifik värme (enheter J/kg∙K) ∆ är en symbol som betyder "förändringen i"
Folk frågar också, vad är förändringen i entalpi för en kemisk reaktion?
För en kemisk reaktion , den entalpi av reaktion (ΔHrxn) är skillnaden i entalpi mellan produkter och reaktanter; enheterna för ΔHrxn är kilojoule per mol. Backa a kemisk reaktion vänder tecknet för ΔHrxn.
Hur definierar du entalpi?
Entalpi är en termodynamisk egenskap hos ett system. Det är summan av den inre energin som adderas till produkten av systemets tryck och volym. Det återspeglar förmågan att utföra icke-mekaniskt arbete och förmågan att frigöra värme. Entalpi betecknas som H; specifika entalpi betecknad som h.
Rekommenderad:
Hur beräknar man standardavvikelsen från PMP?

Formeln som används i PMBOK för standardavvikelse är enkel. Det är bara (P-O)/6. Det är den pessimistiska aktivitetsuppskattningen minus den optimistiska aktivitetsuppskattningen delat med sex. Problemet är att denna form eller form inte på något sätt ger ett mått på standardavvikelse
Hur beräknar man jordens omkrets på dess latitud?

En cirkels omkrets är lika med 2πr där r är dess radie. På jorden är sfärens omkrets vid en given latitud 2πr(cos θ) där θ är latituden och r är jordens radie vid ekvatorn
Hur beräknar man potentialfallet i en krets?
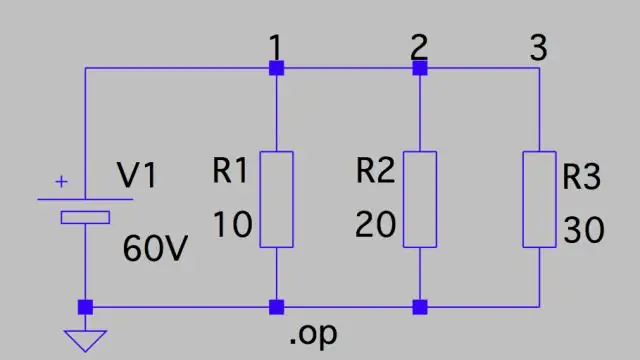
Spänningsfall: Parallell krets Detta betyder att spänningsfallet över var och en bara är kretsens totala spänning dividerat med antalet motstånd i kretsen, eller 24 V/3 = 8 V
Vad är skillnaden mellan allmän kemi och organisk kemi?
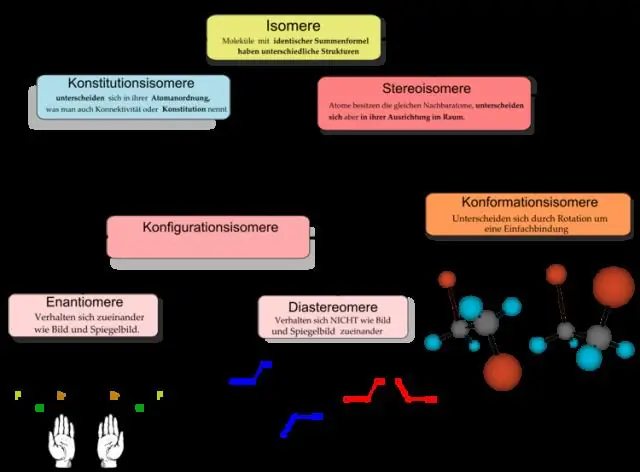
Organisk kemi anses vara en underdisciplin av kemi. Medan den allmänna paraplytermen "kemi" avser sammansättningen och omvandlingarna av all materia i allmänhet, är organisk kemi begränsad till studiet av endast organiska föreningar
Hur beräknar man nedbrytning i kemi?

En nedbrytningsreaktion uppstår när en reaktant bryts ner i två eller flera produkter. Den kan representeras av den allmänna ekvationen: AB → A + B. I denna ekvation representerar AB reaktanten som startar reaktionen, och A och B representerar reaktionens produkter
