
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:41.
- Senast ändrad 2025-01-22 17:10.
Den idealiska gaslagen är, som man säger, faktiskt PV = nRT , med alla standardvariabler. Här är n=m/M, där m är gasens massa och M är gasens molekylvikt. Kort sagt R in PV = nRT skalas ner med faktor M (molekylvikt) för att få in R PV = mRT.
Helt enkelt så, vad är r lika med i pV nRT?
Den ideala gaslagen är: pV = nRT , där n är antalet mol, och R är universell gaskonstant. Värdet av R beror på de inblandade enheterna, men anges vanligtvis med S. I.-enheter som: R = 8,314 J/mol. Det betyder att du kan använda värdet för luft R = 287 J/kg.
Likaså, vad står R för i kemi pV nRT? Universella gaskonstantens enheter R härledd från ekvation PV=n R T. den står för Regnault.
Vad står N för i detta avseende i pV nRT?
. En fysikalisk lag som beskriver förhållandet mellan de mätbara egenskaperna hos en idealgas, där P (tryck) × V (volym) = (antal mol) × R (gaskonstant) × T (temperatur i Kelvin). Det härrör från en kombination av gaslagarna för Boyle, Charles och Avogadro. Kallas även universell gaslag.
Vad är M i idealgaslag?
Originalet idealgaslagen använder formeln PV =nRT, densitetsversionen av idealgaslagen är PM = dRT, där P är tryck mätt i atmosfärer (atm), T är temperatur mätt i kelvin (K), R är idealgaslagen konstant 0,0821 kl m (L) m ol(K) precis som i den ursprungliga formeln, men M är nu molmassan (g m ol
Rekommenderad:
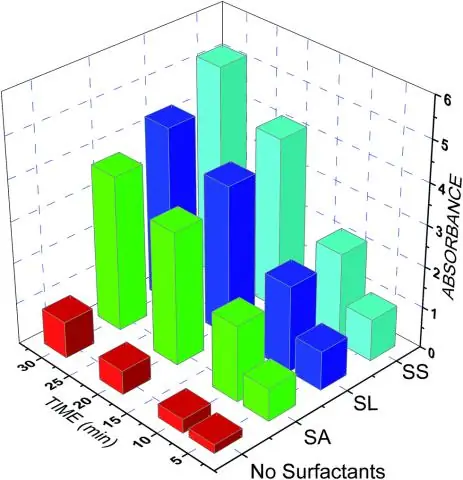
Vad är skillnaden och likheten mellan kolonnkromatografi och TLC?
Den huvudsakliga "skillnaden mellan" dessa två är att "tunnskiktskromatografi" använder en annan stationär fas än kolonnkromatografi. En annan skillnad är att "tunnskiktskromatografi" kan användas för att särskilja icke-flyktiga blandningar, vilket inte är möjligt vid kolonnkromatografi
Vad är skillnaden mellan alfa och beta och gamma?

Alfa-partiklar är energiska (snabba) heliumkärnor, beta-partiklar är mindre och har halva laddningen, eftersom de är energiska elektroner (eller positroner) endast gamma-partiklarna är fotoner, dvs de är inga massiva partiklar alls, de är en form av elektromagnetiska strålning, en form som är mer energisk än röntgenstrålning
Vad är skillnaden mellan Arrhenius-definitionen och Brønsted Lowry-definitionen av syror och baser?

Skillnaden mellan de tre teorierna är att Arrhenius-teorin säger att syrorna alltid innehåller H+ och att baserna alltid innehåller OH-. Medan Bronsted-Lowry-modellen hävdar att syror är protondonatorer och pronacceptorer så baser behöver inte innehålla OH- så syror donerar en proton till vatten och bildar H3O+
Vad är en strukturformel Vad är skillnaden mellan en strukturformel och en molekylär modell?
En molekylformel använder kemiska symboler och subskript för att indikera det exakta antalet olika atomer i en molekyl eller förening. En empirisk formel ger det enklaste, heltalsförhållandet av atomer i en förening. En strukturformel indikerar bindningsarrangemanget för atomerna i molekylen
Vad är skillnaden mellan mikroevolution och makroevolution. Vilka är några exempel på var och en?

Mikroevolution vs makroevolution. Exempel på sådana mikroevolutionära förändringar skulle inkludera en förändring i en arts färg eller storlek. Makrovolution, däremot, används för att hänvisa till förändringar i organismer som är tillräckligt betydande för att de nyare organismerna med tiden skulle betraktas som en helt ny art
