
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Senast ändrad 2025-01-22 17:10.
Storleken av argon är större än klor på grund av de interelektroniska repulsionerna börjar ske när en atom uppnå sin oktett. Argon atom är större än klor atom eftersom, klor atom har 3 yttersta skal som snurrar runt den och den har sju valenselektroner och dess valens är 1.
Och varför är argons atomradie större än alla medlemmar i tredje perioden?
Detta beror på att antalet protoner ökar (natrium har 11, argon har 18) så kärnladdningen ökar. Därför ökar attraktionen mellan den positiva kärnan och negativa elektroner i det yttre skalet, så att Atom radie (avståndet mellan kärnan och det yttre skalet) minskar.
Därefter är frågan varför argon inte följer atomradietrenden? Lägg märke till att argon ingår inte. Elektronegativitet handlar om tendensen hos en atom att attrahera ett bindande elektronpar. Eftersom argon bildar inga kovalenta bindningar, du uppenbarligen burk inte tilldela det en elektronegativitet. De trend förklaras på exakt samma sätt som trend i atomradier.
Utöver detta, vilket grundämne i period tre har den största atomradien?
(B) Trender i atomradien för element under period 3
| Element | Na | Mg |
|---|---|---|
| Enkel elektronkonfiguration | 2, 8, 1 | 2, 8, 2 |
| Energinivån fylls (Valence Shell) | tredje (M) | tredje (M) |
| Kärnladdning (laddning på alla protoner) | 11+ | 12+ |
| Atomradius (pm) | 154 | 130 |
Vad är atomradien för argon?
188 pm
Rekommenderad:
Vilket är förhållandet mellan volym och yta när ett föremål blir större?
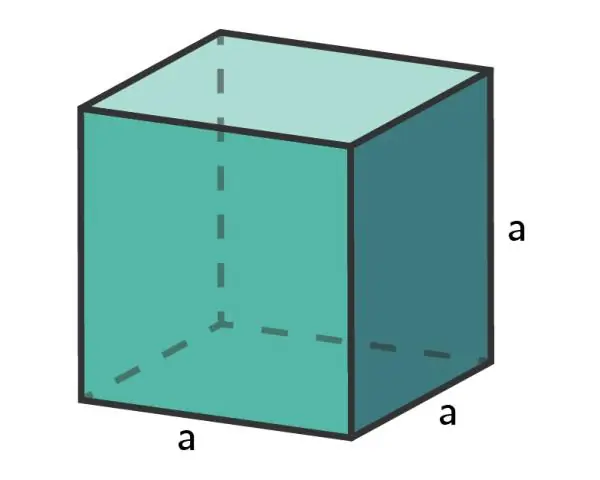
När kubstorleken ökar eller cellen blir större, minskar förhållandet ytarea till volym - SA:V-förhållandet. När ett objekt/cell är mycket litet har det ett stort förhållande mellan ytarea och volym, medan ett stort föremål/cell har ett litet förhållande mellan ytarea och volym
Varför är litiums andra joniseringsenergi så ovanligt större än den första?

Andra joniseringsenergier är alltid högre än den första på grund av två huvudorsaker: Du tar bort elektronen från en position där den ligger något närmare kärnan och därför är föremål för större attraktion till kärnan
Vilken har större bindningsvinkel nh3 eller nf3?
NH3-bindningsvinkeln är 107°. NF3-bindningsvinkeln är 102°. Det finns mer distorsion än för NH3 eftersom enkelbindningarna tar upp mindre utrymme, nära kvävet. Fluor är mer elektronegativt än väte och elektrontätheten i N–F-bindningen är snedställd mot fluoret
Varför är djurceller större än växtceller?

Vanligtvis är växtceller större jämfört med djurceller eftersom de flesta mogna växtceller innehåller en stor central vakuol som upptar majoriteten av volymen och gör cellen större men central vakuol är vanligtvis frånvarande i djurceller. Hur skiljer sig cellväggarna i en djurcell från en växtcell?
Varför är eukaryota genom större?

Genfamiljer och pseudogener En annan faktor som bidrar till den stora storleken på eukaryota genom är att vissa gener upprepas många gånger. Medan de flesta prokaryota gener endast representeras en gång i genomet, finns många eukaryota gener i flera kopior, så kallade genfamiljer
