
- Författare Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Senast ändrad 2025-01-22 17:10.
Isotoper är atomer med samma antal protoner men som har olika antal neutroner. Eftersom atomnumret är lika med antalet protoner och atommassan är summan av protoner och neutroner, burk säg det också isotoper är grundämnen med samma atomnummer men olika massatal.
Vad är isotoper och exempel i detta avseende?
Grundämnen definieras av antalet protoner i atomkärnan. För exempel , måste en atom med 6 protoner vara kol, och en atom med 92 protoner måste vara uran. Förutom protoner innehåller atomerna i nästan varje grundämne också neutroner. Dessa isotoper kallas kol-12, kol-13 och kol-14.
Vet också hur man räknar ut isotoper? Massnumret kan också skrivas som en upphöjd skrift framför elementsymbolen såsom ^235U. Massantalet för en isotop representerar massan av isotoper protoner och neutroner. Beräkna antalet neutroner i an isotop , genom att subtrahera atomnumret från masstalet.
Också att veta, hur bildas en isotop?
Varje kombination av ett grundämne med olika antal neutroner kallas an isotop . Isotoper som är radioaktiva sönderfaller eller sönderfaller på ett förutsägbart sätt och i en viss hastighet att göra Övrig isotoper . Den radioaktiva isotop kallas föräldern och den isotop bildad av förfallet kallas dottern.
Vad är en isotoplätt definition?
isotop . Ett isotop av ett kemiskt element är en atom som har ett annat antal neutroner (det vill säga en större eller mindre atommassa) än standarden för det elementet. Atomnumret är antalet protoner i en atoms kärna.
Rekommenderad:
Vad är skillnaden mellan allmän kemi och organisk kemi?
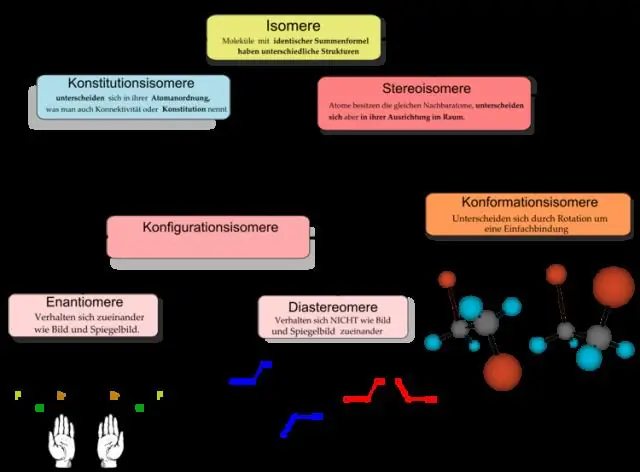
Organisk kemi anses vara en underdisciplin av kemi. Medan den allmänna paraplytermen "kemi" avser sammansättningen och omvandlingarna av all materia i allmänhet, är organisk kemi begränsad till studiet av endast organiska föreningar
Hur använder man Aufbau-principen i kemi?

Aufbau-principen beskriver reglerna som används för att bestämma hur elektroner organiseras i skal och underskal runt atomkärnan. Elektroner går in i underskalet med lägsta möjliga energi. En orbital kan innehålla högst 2 elektroner enligt Paulis uteslutningsprincip
Hur beräknar man entalpiförändring i kemi?

Använd formeln ∆H = m x s x ∆T för att lösa. När du har m, massan av dina reaktanter, s, din produkts specifika värme och ∆T, temperaturförändringen från din reaktion, är du beredd att hitta reaktionsentalpin. Anslut bara dina värden till formeln ∆H = m x s x ∆T och multiplicera för att lösa
Hur introducerar man isotoper?
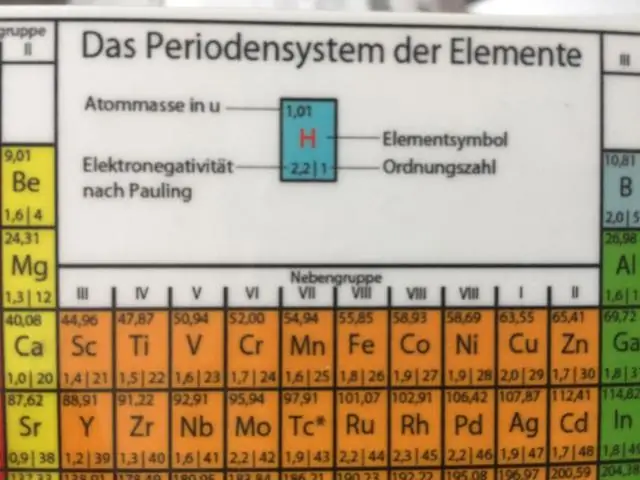
Isotoper definieras först av deras element och sedan av summan av de närvarande protonerna och neutronerna. Kol-12 (eller 12C) innehåller sex protoner, sex neutroner och sex elektroner; därför har den ett massatal på 12 amu (sex protoner och sex neutroner)
Hur beräknar man nedbrytning i kemi?

En nedbrytningsreaktion uppstår när en reaktant bryts ner i två eller flera produkter. Den kan representeras av den allmänna ekvationen: AB → A + B. I denna ekvation representerar AB reaktanten som startar reaktionen, och A och B representerar reaktionens produkter
